까다로운 암세포 찾아가
활성산소 만드는 똑똑한 접합체 개발
KRAS 돌연변이 췌장암 생쥐모델에서 항체-광응답제의 암세포사멸 효과 확인
췌장암은 다른 암 종에 비해 비교적 드물게 발생하는 암이나 생존율이 저조한 질병이다. 생존율 향상을 위해서는 조기에 수술하는 것이 중요하나 췌장이 복부 깊숙이 위치해 접근이 어렵고, 증상이 없어 조기 발견이 힘들다. 췌장암을 표적하여 사멸을 유도하는 표적항암제가 있으나 대부분의 췌장암 유전자가 변형되어 듣지 않는 한계점이 있다. 이에 착안하여 기존 치료법에 차도를 보이지 않거나 치료법이 부재한 췌장암의 환자들의 고통을 줄이고 삶의 질을 향상시키는 연구가 필요하다.
암세포를 찾아갈 수 있는 네비게이션 역할을 하는 항체(antibody)를 항암제에 접목한 치료제 시장이 성장하는 가운데 항암제를 광응답제로 치환한 연구결과가 나왔다.
빛에 반응해 주변 세포에 스트레스가 되는 활성산소를 생성하는 광응답제와 암세포 표면의 생체고분자에 결합하는 항체를 접합시킨 것이다. 광응답제를 이용한 광역학 치료와 단일클론항체를 이용한 항체 치료는 그간 단독으로 암을 치료하는데 사용되어 왔다.
가톨릭대학교 나건 교수 연구팀이 돌연변이 췌장암 세포를 표적으로 면역반응과 산화스트레스에 의한 세포사멸과정을 함께 활성화하기 위한 항체-광응답제 접합체를 개발했다고 밝혔다.
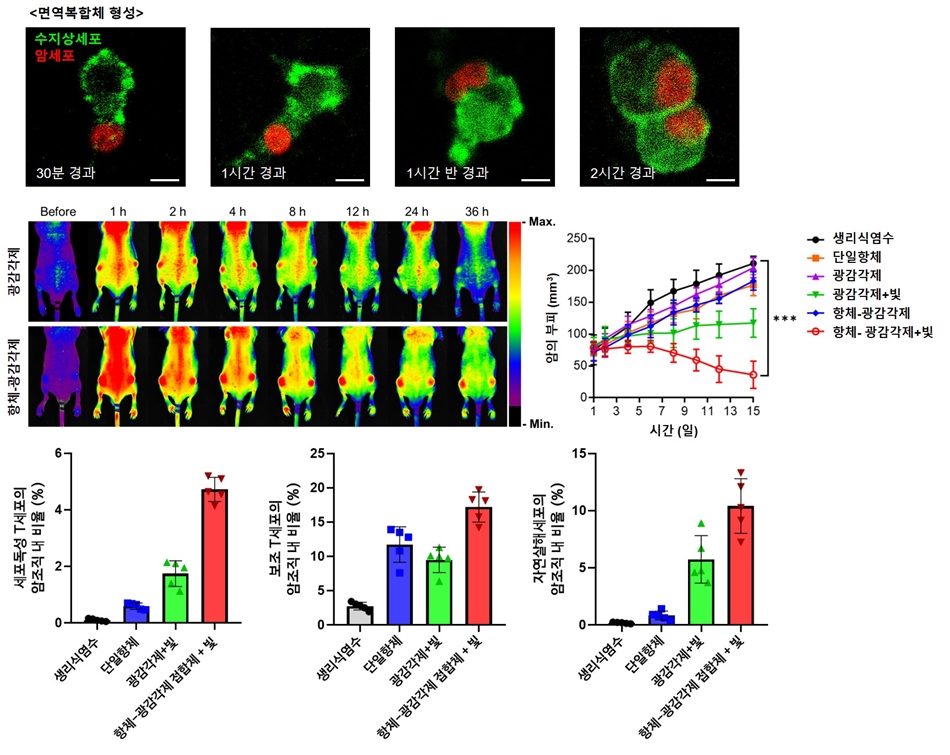
연구팀이 제작한 이 접합체를 췌장암 모델 생쥐에 주사하고 암 조직에 빛을 쬐어준 결과 종양의 크기가 대조군 대비 5배 감소한 것으로 나타났다.
항암면역 치료에 중요한 면역세포(수지상세포, T세포, 자연살해세포)가 항체 단일치료에 비해 평균 6배, 광역학 단일치료에 비해 평균 2배 가량 더 많아져 면역활성이 높아진 것으로 나타났다.
전이성 췌장암에 사용되는 항체는 암세포 표면의 수용체(표피성장인자 수용체)에 결합함으로써 암세포를 인식할 뿐만 아니라 암세포 내의 성장신호 전달을 막는 방식으로 작동한다.
하지만 췌장암 환자의 95%에서 나타나는 돌연변이 유전자(KRAS 유전자의 특정 염기 변이)를 가진 암세포의 경우, 이러한 항체는 암세포를 찾아갈 수 있지만 암세포 성장신호를 차단하지는 못한다. 따라서 일반적인 항체-항암제 접합체의 경우 항암제가 항체로부터 방출되면서 항암효과를 나타낸다.
연구팀이 개발한 항체-광응답제 접합체는 기존 항체-항암제 접합체처럼 표적과 공격 두 가지 기능을 하나에 담되, 성공적인 공격에 영향을 미칠 수 있는 요소들을 간소화하였다.
암세포 안으로 유입되지 않고 표면에서도 작용할 수 있고, 항체로부터 광응답제가 분리될 필요도 없이 빛을 쬐는 것만으로 암세포 표면에서 암세포를 공격할 수 있다는 설명이다.
기존 접합체는 일단 암세포 안으로 유입되어야 하며, 유입된 후에도 항체로부터 약물이 제대로 분리되어야 약물이 암세포를 공격할 수 있는 방식이었다.
KRAS 변이 췌장암세포에 대한 항체 접목 광역학 치료의 실마리가 될 이번 연구는 현재 비임상 시험을 통한 효과규명 단계로 연구팀은 향후 기술이전 또는 창업을 통한 임상에 적용할 수 있는 제품개발을 추진할 계획이라고 밝혔다.
과학기술정보통신부와 한국연구재단이 추진하는 중견연구사업의 지원으로 수행된 이번 연구의 성과는 국제학술지‘스몰(Small)’에 2월 16일 게재되었다.
논문명은 Immune Stimulating Antibody‐Photosensitizer Conjugates via Fc‐Mediated Dendritic Cell Phagocytosis and Phototriggered Immunogenic Cell Death for KRAS ‐ Mutated Pancreatic Cancer Treatment이다.
주요내용 설명
<작성 : 가톨릭대학교 나건 교수>
논문명
Immune Stimulating Antibody‐Photosensitizer Conjugates via Fc‐Mediated Dendritic Cell Phagocytosis and Phototriggered Immunogenic Cell Death for KRAS ‐ Mutated Pancreatic Cancer Treatment
저널명
Small
키워드
antibody-photosensitizer conjugate(항체 광응답제 접합체), cetuximab(세툭시맙), immune complex(면역 복합체), immunotherapy(면역치료), photodynamic therapy(광역학 치료)
DOI
10.1002/smll.202006650
저 자
나건 교수(교신저자/가톨릭대학교), 김다혜 박사(제1저자/가톨릭대학교), 이상희(가톨릭대학교)
1. 연구의 필요성
○ 췌장암은 생존율 12%로 조기진단의 어려움으로 인해 대개 처음 진단 시 여러 장기에 퍼져있을 가능성이 높아 환자의 20% 정도만 수술을 받을 수 있다. 최근 췌장암 표적치료에 췌장암 세포의 성장을 억제하는 단일클론 항체(monoclonal antibody)가 급부상하고 있다.
○ 전이성 췌장암 치료를 위해 화학항암제와 병용하여 쓰이는 세툭시맙 (Cetuximab)은 표피 성장인자 수용체(epidermal growth factor receptor, EGFR)에 결합하여 암세포 성장을 억제하는 항체이다. 성장인자와 경쟁적으로 수용체에 부착하여 암세포 성장을 위한 신호전달을 억제해 사멸시킨다.
○ 최근 차세대 항암전략으로 항체약물접합체(Antibody-drug conjugate, ADC) 가 부각되고 있다. 암세포의 특정 단백질 혹은 수용체에 결합할 수 있는 항체에 약물을 붙이고, 이를 암 세포에 보내 표적 부위에만 약물을 전달하는 기술이다. 시장조사 분석기관 이밸류에이트파마에 따르면, 2020년 기준 글로벌 시장규모 약 26억 달러(한화 약 2조 9400억원) 규모로 파악된다.
○ 한편 췌장암 환자의 95%가 변이된 KRAS 유전자에 의해 기존 항체 약물접합체를 이용한 치료에 효과가 없는 것으로 밝혀지고 있다.
※ KRAS(Kristen Rat Sarcoma virus) 돌연변이 : 종양의 성장과 증식에 관여하는 암 유발 유전자. 폐암, 대장암, 췌장암등 다양한 암종의 원인이 되며, KRAS 변이는 전이성 암에서 흔히 관찰된다.
○ 이에 연구팀은 항체 및 광역학치료를 병용할 수 있는 항체-광응답제 접합체(Antibody-photosensitizer conjugates, APC)를 개발했다. 이는 항체-수용체 결합으로 암세포에만 특이적으로 달라붙는다. KRAS 돌연변이가 일어났음에도 불구하고 항체에 접합된 광응답제가 빛을 받아 생성된 활성산소로 암세포를 사멸시킨다.
○ 더불어 항체약물접합체의 경우 세포 내에서 링커에 의해 연결된 약물이 분리되어야만 활성을 기대할 수 있다. 하지만 항체 광응답제 접합체의 경우 분리과정 없이 빛에 의한 활성산소로 극대화된 효과를 기대할 수 있다.
○ 항체-광응답제 접합체(APC)는 빛을 이용한 선택적 광역학치료와 면역 치료 두 가지 효과를 동시에 얻을 수 있을 것으로 기대하고 있다.
○ 항원(암세포)-항체 복합체가 면역활성에 중요한 역할을 하는 수지상 세포에 빠르고 정확하게 인식되도록 함으로써 암 환경의 면역 회피 경로를 막을 수 있다. 또 광역학치료 매개 면역을 활성화할 수 있다.
2. 연구내용
○ 연구팀은 기존 표적 항암치료가 어려운 KRAS 돌연변이 췌장암의 병용치료 전략으로 항체 광응답제 접합체를 개발했다.
○ 췌장암 세포 90%에서 과발현하는 표피 성장인자 수용체를 선택적으로 저해하는 세툭시맙과 광역학 치료에 사용되는 광응답제를 화학적으로 접합한 것이다.
○ 접합체는 표피성장인자 수용체가 발현된 췌장암 세포에 선택적으로 달라붙고, 항체에 결합되어 있는 광응답제는 빛에 반응해 만들어내는 활성산소로 효과적인 암세포 사멸을 일으킨다.
○ 암세포의 항원과 항체의 결합은 면역복합체를 형성하는데 이는 면역세포에 성공적으로 탐식됨으로써 빠르고 정확한 면역작용을 유발한다.
※ 면역복합체(immune complex) : 항체는 구조적 특성상 Fc 부분과 Fab 부분으로 나눌 수 있다. Fab 부분은 암세포에 결합, Fc 부분은 면역활성에 주요한 역할을 하는 수지상세포에 결합된다. 면역복합체는 자가항원인식 효과로 면역활성을 유도 한다.
○ 실제 췌장암 생쥐모델에 항체-광응답제 접합체를 주사하고 빛을 쬐어 치료효과를 확인했다. 암 크기는 대조군보다 약 5배 감소하였다. 또한 광역학 매개 면역활성 효과로 광역학 단일 치료보다 수지상세포의 성숙은 1.64배, 세포독성 T세포는 2.71배 증가한 것을 확인했다.
3. 연구성과/기대효과
○ 개발한 항체-광응답제 접합(APC)는 KRAS 돌연변이와 무관하게 작용 할 수 있다. 항체를 통해 암세포를 표적하고 광역학 치료를 통해 기존 항체약물접합체(ADC) 치료로 접근이 어려웠던 돌연변이 췌장암에 접근하고자 하였다.
○ 또한 접합체 제조를 위한 화학적 합성 기법은 췌장암 뿐 아니라 다양한 암세포를 표적할 수 있는 항체나 다양한 성질의 광응답제에 확대 적용할 수 있을 것으로 연구팀은 기대하고 있다.
□그림 설명
 |
(그림 1) 개발한 항체-광응답제 접합체를 이용한 암 표적 치료 전략의 개략도
췌장암 표면에 과발현된 수용체에 항체-광응답제가 부착한 후 빛 조사에 의한 광역학 암세포 사멸을 유도할 수 있다. 암세포가 사멸하면서 방출하는 면역원성 인자에 의해 주변 면역세포의 성숙을 야기하여 암 미세환경의 면역활동을 활성화한다. 또한 항체의 Fab 부분과 암 항원의 부착으로 인한 면역복합체 형성이 주변 항원제시세포에 성공적으로 탐식되어 빠르고 효과적으로 암세포에 대한 면역능이 증강한다.
그림설명 및 그림제공 : 가톨릭대학교 나건 교수
 |
(그림 2) 암세포-항체 면역복합체의 수지상세포내로의 포식과정과 면역유도 효과
항체-광응답제는 항원(암세포)-항체 면역복합체를 형성하고, 주변 미성숙 수지상세포에 인식 및 포식되어 다른 면역세포의 활성을 유도한다. 췌장암 생쥐 모델에 항체-광응답제를 주사하면 광응답제에 비해 암세포에 특이적으로 축적되며, 빛 조사를 통해 암을 성공적으로 치료한다. 또한, 암 조직 내 여러 면역세포를 모집하여 암을 공격하는 것을 입증하였다.
그림설명 및 그림제공 : 가톨릭대학교 나건 교수
□연구자 소개
나 건 교수, 교신저자
 |
1. 인적사항
○ 소 속 : 가톨릭대학교 바이오메디컬화학공학과
○ 전 화 : 02-2164-4832
2. 학력
○ 1989 전남대학교 학사(공업화학)
○ 1992 전남대학교 석사(공업화학)
○ 1997 전남대학교 박사(공업화학)
3. 경력사항
○ 2005 ~ 현재 가톨릭대학교 교수(바이오메디컬화학공학과, 생명공학과)
○ 2006 ~ 2007 미국유타대학교 방문 교수(약학 및 약품화학과)
○ 2019 ~ 2020 한국 공업화 학회 생체재료분과 분과회장
○ 2015 ~ 현재 한국 생체재료 학회 부회장
○ 2017 ~ 2019 한국 과학기술정보통신부 국가과학기술심의회 전문위원
○ 2017 ~ 현재 한국 식품의약품안전처 의료기기 전문위원
○ 2018 ~ 2020 한국연구재단 기초연구본부 공학단 전문위원
4. 전문분야 정보
○ 생체재료, 암 치료 및 진단, 약물 전달체, 면역치료
5. 연구지원 정보
○ 2017 ~ 현재 과학기술정보통신부‧한국연구재단 기초연구사업(중견연구)
김 다 혜, 제1저자
 |
1. 인적사항
○ 소 속 : 가톨릭대학교 바이오메디컬화학공학과
○ 전 화 : 02-2164-4918
2. 학력
○ 2016 가톨릭대학교 학사(생명공학)
○ 2020 가톨릭대학교 박사(생명공학)
○ 2020 가톨릭대학교 박사후 연구원(생명공학)
3. 경력사항
○ 2017.10.20 추계 한국생체재료학회 우수 논문 발표상
○ 2019.03.22 한국중재의료기기학회 포스터 발표 우수상
4. 전문분야 정보
○ 나노/마이크로 약물전달 제형 설계, 항체-약물 접합체, 면역치료, 항암치료
한구연구재단 홍보실 제공
노벨사이언스 science@nobelscience.co.kr
<저작권자 © 노벨사이언스, 무단 전재 및 재배포 금지>



 간단한 공정으로 이산화탄소 분리 성공
간단한 공정으로 이산화탄소 분리 성공








