인간 소장 상응 약물 흡수 및 대사 평가 기능 모델 개발
3차원 장 오가노이드 전환기술개발 통한 인체반응 예측률 향상에 기여
 |
| 연구팀 |
국내연구진이 세계 최초로 인간 소장 상피 모델을 개발했다. 인간의 몸을 구성하는 다양한 세포로 분화할 수 있는 능력을 가진 세포에서 유래된 인간 소장 상피 모델 제작 기술은 2차원 직접 분화 또는 3차원 오가노이드에서 2차원 소장 상피 세포로 전환이 가능해 활용성이 기대되고 있다. 또한 인체의 장과 유사한 세포 다양성과 기능성을 가져, 소장에서의 약물 흡수 및 대사 평가가 가능한 플랫폼 기술로써 향후 신약개발에 큰 기여를 할 것으로 기대된다.
생명硏 손미영 박사팀이 수행한 이번 연구는 과학기술정보통신부와 한국연구재단의 Korea Bio Grand Challenge 사업, 산업통상자원부의 바이오산업기술개발과 3D생체조직칩 기반 신약개발 플랫폼 구축사업, 생명硏의 Research Initiative Program의 지원으로 수행되었고, 미국과학진흥회(AAAS)에서 발행하는 종합과학 분야의 세계적 권위지인 사이언스 어드밴시즈(Science Advances)지에 6월 2일자에 게재되었다.
분화인자 이용, 인간소장조직 모사한 고성능 소장 상피 모델 개발 성공
연구팀은 인간 전분화능줄기세포의 직접 분화 혹은 3차원 오가노이드 전환기술을 이용한 고성능 인간 소장 상피 모델을 개발하였다. 신약개발을 위해서는 약물이 우리 몸에서 순환하는 일련의 과정에 대한 분석이 중요하다. 이를 위해 후보 약물의 흡수, 분포, 대사, 배설(ADME)에 대한 약물동태 평가가 필요하다. 지금까지는 소장에서의 약물 흡수도를 평가하기 위해 절대표준(Gold Standard)으로 대장암 조직에서 유래한 장 세포를 사용하고 있지만, 인체 소장을 동일하게 구현하지 못하여, 소장에서 일어나는 약물의 흡수와 1차 대사를 평가하고 예측하는 것에 한계점이 있었다.
 |
최근 전분화능줄기세포로부터 소장 세포로 분화시키는 기술이 보고되고 있으나, 낮은 분화도와 세포 다양성 부재로 인해 기능성이 떨어지며, 대량 증식의 어려움이 있었다.
생명硏 손미영 박사 연구팀은 기존 문제를 극복하고, 인간 소장에 존재하는 다양한 세포 구성과 기능성 구현을 위해, 소장 상피 세포 전구체를 이용해 대량 배양 및 동결보관이 가능하게 하였고, 새롭게 발굴한 분화인자를 이용하여 높은 수준으로 인간 소장 조직을 모사할 수 있는 고성능 소장 상피 모델 개발에 성공하였다.
또한, 연구팀은 환자 유래 역분화줄기세포를 이용하여 환자 맞춤형 약물 효능 평가 시스템 개발의 가능성을 검증하였으며, 3차원 장 오가노이드를 2차원 소장 상피 세포 모델로 전환할 수 있는 기술 개발을 통해 본 모델 시스템의 범용성을 확인하였다.
“신약개발 및 고기능성 3차원장 오가노이드 활용 기반 기술될 것”
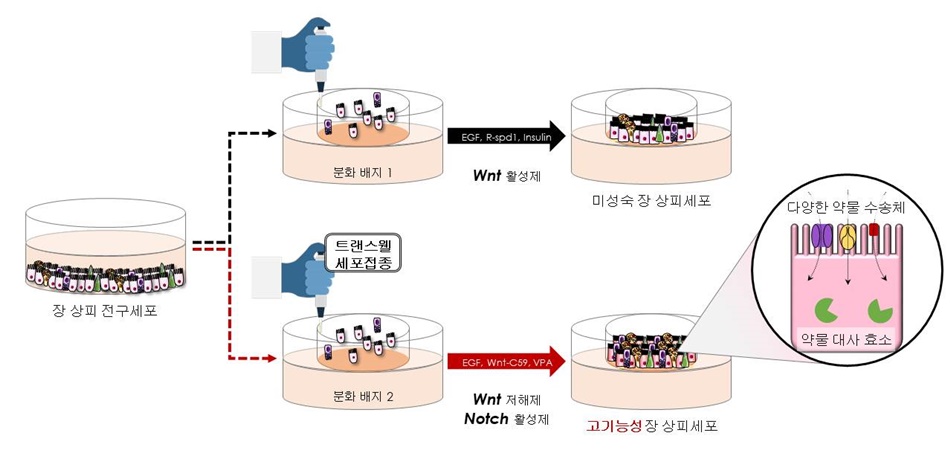
연구팀은 새로운 분화 기법 개발을 통해 전분화능줄기세포로부터 대량 증식 및 동결보관이 가능한 소장 상피 세포 전구체 분화법을 구축하였으며, WNT 신호 저해제와 NOTCH 신호 활성제를 이용한 소장 상피 세포 전구체의 추가적인 분화 유도를 통해 고성능 소장 상피 모델을 개발에 성공하였다.
연구팀은 “고성능 소장 상피 모델은 실제 소장 상피에 존재하는 세포들과 비슷한 수준의 특이적 유전자 및 단백질 마커를 발현하며, 약물 흡수 및 대사에 중요한 효소의 활성을 나타내었으며, 장 내 대표적 분화세포인 흡수 세포(enterocyte), 배상 세포(goblet cell), 파네스 세포(paneth cell), 내분비세포(enteroendocrine cell)를 모두 포함한 소장 조직을 모사할 수 있는 세포 모델임을 검증하였다”고 말했다.
이어 “전분화능줄기세포로부터 확립된 고성능 소장 상피 세포 모델 분화 기법은 3차원 오가오이드로부터 2차원 소장 상피 세포로의 전환 기술에 적용 가능하며, 환자 유래 역분화 줄기세포를 이용한 소장 상피 세포 분화에도 적용이 가능한 범용성이 있는 기술로 향후 환자 맞춤형 약물 평가 모델 시스템 개발이 가능한 것으로 확인되었다”고 밝혔다.
 |
고성능 소장 상피 모델은 약물의 흡수도 평가 시, 소장에서의 1차 대사를 반영할 수 있는 유일한 소장 상피 모델로써 실제 인간 소장에서의 약물 흡수도와 유사한 결과를 나타내어 차후 새로운 신약 개발 플랫폼으로써 활용될 수 있으며, 장내미생물 공배양 또는 면역세포 공배양도 가능함을 확인함에 따라 다양한 생물학적 실험에 광범위하게 활용할 수 있을 것으로 기대된다.
줄기세포융합연구센터 손미영 박사는 “본 연구팀의 고성능 인간 소장 상피 모델은 소장 조직을 모사할 수 있는 세계 최고 수준의 모델로 높은 정확도의 약물 흡수·대사 평가를 통해 신약의 효율을 나타내는 지표인 생체이용률(bioavailability)을 예측하고 약효 개선에 활용될 수 있다”며, “인체 조직 수준의 세포모델 개발, 대량화 기술 및 관련 평가법 개발은 향후 신약 개발 과정에 효과적으로 기여할 수 있고, 또한 본 연구팀이 이미 확보하고 있는 고기능성 3차원 장 오가노이드를 더욱 다양하게 활용하기 위한 기반 기술로도 기대된다”고 밝혔다.
 |
<Q&A>
Q. 이번 성과 뭐가 다른가
A. 기존의 개발된 장 상피 세포 모델은 낮은 분화도 및 기능성으로 인해 약물의 흡수 및 1차 대사 평가의 정확도가 낮았고, 실험 배치(batch) 간 차이가 심하고, 대량 배양 및 동결보관이 어려움에 따라 활용에 있어 제한적이었다. 본 연구진이 새롭게 개발한 소장 상피 세포 모델은 대량 증식 및 동결보관이 가능하고, 실제 인간 소장 조직의 상피 세포를 비슷한 수준으로 모사함에 따라 넓은 활용성을 지니며, 높은 정확도로 약물의 흡수 및 1차 대사 평가가 가능하다.
Q. 어디에 쓸 수 있나
A. 본 연구진이 개발한 소장 상피 모델은 약물의 생체이용률 평가 및 이에 따른 효능 및 독성 예측에 이용될 수 있으며, 나아가 신약 개발을 위한 플랫폼 기술로 활용이 가능하다. 또한, 환자 유래 역분화 줄기세포를 이용한 환자 맞춤형 약물 평가가 가능하며, 장내미생물 또는 면역세포와의 공배양을 통한 다양한 생물학적 연구에도 적용이 가능할 것으로 기대된다.
Q. 실용화까지 필요한 시간은
A. 본 연구결과는 고성능 소장 상피 세포 모델을 제시하는 최초의 보고로 현재 SOP(표준작업절차서) 제작 및 실험실간 교차 검증을 통한 기술 표준화를 진행 중에 있으며, 향후 사업화 전략을 통해 표준 기술 개발 및 상용화를 추진할 계획이나, 신약 개발 과정에서 대체 시험법 개발은 기존 약물 평가 및 신약 개발 플랫폼을 넘어서는 안전성, 재현성 획득이 필요하므로 많은 소요시간이 필요할 것으로 예상된다.
Q. 실용화를 위한 과제는
A. 소장 상피 세포 모델로써 실용화하기 위해서는 대량 증식 및 동결보관을 통해 세포를 안정적으로 공급 가능하고, 배치 간 차이 없이 항상 고기능성을 유지할 수 있는 재현성 있는 세포 배양 기술이 필요하다. 따라서, 표준화 작업을 통해 일정한 성능의 고기능성 소장 상피 세포 생산 절차 확립이 필요하고, 나아가 약물 흡수 및 대사 평가 시스템의 표준화로 확장이 필요하다. 이를 위해 향후 지속적인 연구를 통해 실용화를 위한 기술 표준화를 완성 할 계획이다.
Q. 연구를 시작한 계기는
A. 기존의 소장 상피 세포 모델은 암 세포 유래 세포주(cell line)를 이용한 경우가 주로 사용되고 있고, 최근 들어 전분화능줄기세포를 이용한 장 상피 세포 분화 기법들이 일부 보고 되었다. 하지만, 현재까지 개발된 장 상피 세포 모델은 분화도가 낮고, 기능성이 떨어져 실제 약물 흡수 및 대사 평가에 활용하기에 한계가 있었다. 따라서, 높은 수준으로 실제 인간 소장 상피 세포를 모사하는 고기능성 장 상피 세포를 개발하여 약물의 흡수 및 대사 평가의 정확도를 높이고, 나아가 약물의 효능 (또는 독성)을 효율적으로 평가 및 예측할 수 있는 모델 시스템이 필요하다고 생각하였다.
Q. 에피소드가 있다면
A. 본 연구팀이 개발한 소장 상피 세포 모델은 많은 연구원과 다양한 전문성을 지닌 팀 간의 협업을 통해 이루어졌다. 소장 상피 세포 모델의 다양한 특성 및 기능성을 검증하기 위해 효소 활성 측정 및 면역 염색 등 다양한 연구 방법이 필요하여 많은 연구원들이 본 연구에 참여하였으며, RNA 시퀀싱 및 데이터 분석, 약물 훕수 및 대사 평가, 전자현미경 이미징 분석, 장내 미생물 및 면역세포 공배양 등 새롭게 도전하는 실험들은 전문성을 지닌 다양한 팀과의 열띤 토론과 협업을 통해서 완료할 수 있었다. 일련의 과정들이 매순간 새로운 도전이고 위기였지만 항상 믿고 따라준 팀원들게 감사하며, 헌신적인 배려와 애착을 가지고 본 연구를 완수할 수 있게 도와 준 많은 동료 연구원들게 깊이 감사드린다.
Q. 꼭 이루고 싶은 목표는
A. 기초연구라는 영역에서 오랫동안 머물다 보면 실용화에 대한 생각이 점점 옅어지는 측면이 있다. 본 연구를 시작하고 진행하면서 실제 약물 흡수 및 1차 대사 평가에서 기존에 가장 널리 사용하고 있는 대장암 세포주인 CACO-2 세포 모델에 비해 소장 상피 세포 모델의 우수성을 입증할 때마다 이번 연구는 기초연구를 통해 실용화에 이를 수도 있다는 기대감을 품게 되었다. 따라서, 본 연구팀의 목표는 기초연구 영역에 머무르지 않고, 기초연구를 통해 얻은 성과를 실제 실용화까지 발전시켜 보는 것이 목표다. 과정은 험난하겠지만 실용화에 성공하여 신약 개발 등 다양한 산업 분야에 작은 기여나마 할 수 있길 기원한다.
Q. 신진연구자를 위한 한마디
A. 현대 과학이 점점 복잡해지고 고도화됨에 따라 혼자서 할 수 있는 연구는 점점 줄어들고 있습니다. 현대 과학의 발전에 발맞춰 성장하기 위해서는 팀원들과 그리고 다양한 전문가들과의 협업이 필수적입니다. 지금 시작하는 신진연구자들께서 부디 좋은 인연을 많이 만나 동료연구원들과 창의적인 협업을 많이 하길 바라며, 그로 인해 상생의 연구문화가 뿌리 내리길 바랍니다.
<용어 설명>
1. 전분화능줄기세포 (Pluripotent stem cells)
- 인간의 몸을 구성하는 세포로 분화하는 능력을 가진 세포로서, 전분화능 (pluripotency)과 자기재생능력 (self-renewal)을 가진다. 크게 배아의 내세포집단 (inner cell mass)에서 분리한 배아줄기세포 (embryonic stem cell)와 유도만능 줄기세포 (induced pluripotent stem cell)로 구분된다.
2. 소장 상피 세포 (Small intestinal epithelial cell)
- 소장 상피 세포란 동물의 장을 형성하는 단층원주상피(simple columnar epithelium)를 구성하는 세포로써 흡수 세포(enterocyte), 배상 세포(goblet cell), 파네스 세포(paneth cell), 내분비세포(enteroendocrine cell)를 포함하고 있으며, 영양분의 흡수 및 대사, 외부 병원균 침투 방어 등의 기능을 수행하고 있다.
3. 약물 흡수 및 대사 평가 (Evaluation of drug absorption and metabolism)
- 소장 상피는 약물의 흡수 및 1차 대사가 일어나는 장기로 복용한 약물의 효능 또는 독성을 평가 및 예측하기 위해서는 정확한 약물의 흡수 및 CYP3A4대사효소에 의한 약물의 1차 대사 측정이 필수적이다.
4. 3차원 장 오가노이드 (3D Intestinal organoids)
- 줄기세포로부터 장 특이적 세포로 분화한 세포를 3차원 배양을 통해 다시 응집, 재조합 시켜 만든 장 장기유사체를 말한다.
5. 환자 맞춤형 치료 (Patient-specific treatment)
- 각각의 환자에 대해 어떠한 치료법이 효과가 있는지 결정해 처방을 내리는 개인 맞춤형 의학 모형이다.
6. WNT 신호전달체계 (WNT signaling pathway)
- 생물의 신호전달체계의 일종으로 초기발생과 형태형성에 필수적인 경로이다. WNT는 분비성 단백질로 세포막의 수용체와 결합하여 베타 카테닌(beta-catenin) 경로를 활성화 시키는 것으로 알려져 있다.
7. NOTCH 신호전달체계 (NOTCH signaling pathway)
- 생물의 신호전달체계의 일종으로 대부분의 동물에 보존되어 있다. 포유류에는 4종의 NOTCH 수용체가 존재하며, 동물의 배발생에 필수적이며, 신경계 형성 과정 동안 세포의 분열을 촉진하고 분화를 저해하는 것으로 알려져 있다.
노벨사이언스 김주현 기자 science@nobelscience.co.kr
<저작권자 © 노벨사이언스, 무단 전재 및 재배포 금지>



 간단한 공정으로 이산화탄소 분리 성공
간단한 공정으로 이산화탄소 분리 성공








