ALK 양성 비소세포폐암의 표적항암제 회피 원리 및 제어 기전 규명
향후 항암제 내성 폐암 치료제 개발에 기여 기대
 |
| 연구팀 왼쪽에서 3번째 연구책임자 김미랑 박사, 5번째 제1저자 허해정 박사과정생 |
국내 연구진이 폐암 환자의 항암제 내성 원인을 밝히고 새로운 치료 타겟을 발견하였다. 이를 통해 향후 항암제 내성 암세포를 제거할 수 있는 새로운 치료 전략으로 활용할 수 있을 것으로 기대되고 있다.
한국생명공학연구원 김미랑․김선영 박사 공동연구팀은 단일세포 유전체분석 기술을 이용하여 ALK(Anaplastic Lymphoma Kinase, 역성형 림프종 인산화효소) 양성 비소세포폐암 환자의 항암제 내성 기전을 규명하고, 제어할 수 있는 실마리를 찾았다고 밝혔다.
전체 암 사망자의 22.7% 달하며 사망률이 가장 높은 암종인 폐암은 암세포의 크기와 형태에 따라 소세포폐암과 비소세포폐암으로 구분된다.
현미경으로 확인되는 암세포의 크기가 작은 것은 소세포폐암이라고 하고 작지 않은 것을 비소세포폐암이라고 하며, 전체 폐암 환자의 80~85%이 비소세포폐암에 해당한다.
비소세포폐암 중 약 5% 정도에서 ALK 유전자의 변이로 인한 ALK 양성 비소세포폐암이 발병하며, 주로 50대 이하의 젊은 연령대나 비흡연 폐암환자에게서 발견된다.
 |
| ALK 표적항암제 내성 폐암의 항암제 내성 원인 규명Cytidine deaminase (CDA)를 과발현하는 세포는 항암제를 투여하기 전의 암세포 집단에서도 소수 존재하며, 항암제를 투여하면 항암제로부터 회피하여 활발히 증식함으로써 항암제 내성의 원인이 됨 |
ALK 양성 비소세포폐암은 표적항암제를 투여하면 뛰어난 치료 효과를 보이지만 지속적인 투여 시, 항암제 내성이 생겨 재발과 이후 치료를 더욱 어렵게 한다. 항암제 내성 원인으로 2차 돌연변이가 주목받고 있지만, 아직 그 기전을 모르는 부분이 절반 이상을 차지하고 있다.
최근 유전체 분석기술의 발달로 개별 세포의 유전자 발현 분석이 가능해지며 항암제 내성의 원인이 되는 희귀 암세포를 구별해 내는 연구가 가능해지고 있다. 이에 연구팀은 단일세포 유전체 기술을 통해 항암제 내성 세포의 유전자 발현 변화를 분석하여 내성 원인을 규명하였다.
CDA(Cytidine deaminase, 시티딘 탈아미노효소)는 암세포의 증식과 이동성을 높여 전이를 유발하는 효소로, 표적항암제를 투여하면 암세포 내 CDA가 활성화되어 항암제를 회피하고 증식하며 항암제의 내성이 생긴다는 것이다. 이를 기반으로 연구팀은 CDA를 억제제를 이용하여 내성이 생긴 암세포만 선택적으로 사멸시킬 수 있다는 사실을 확인하였다.
연구책임자인 김미랑 박사는 “본 연구 결과가 임상에 실제로 적용되기 위해서는 안전성 및 유효성 등 여러 검증 절차와 많은 연구가 필요하지만, 암 환자의 생존율을 높이는데 조금이라도 기여할 수 있으면 좋겠다”고 밝혔다.
이번 연구는 생화학분자생물학회 국제저널인 Experimental and Molecular Medicine(IF 12.178), 2022년 8월 23일자 온라인 판에 게재되었다.
이 연구는 과학기술정보통신부 포스트게놈유전체사업, 산업통상자원부 유전자의약산업진흥 유전체분석시스템구축사업, UST Young Scientist 양성사업, 그리고 생명연 주요사업의 지원으로 수행되었다.
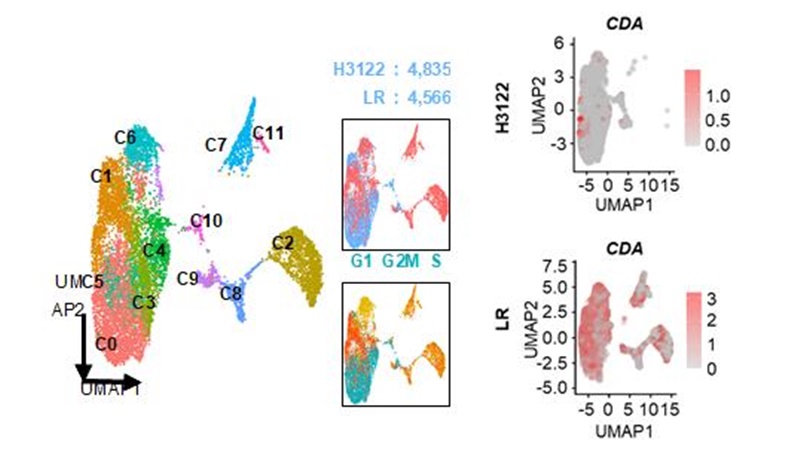 |
| ALK 표적항암제 내성 폐암 세포의 단일세포 유전체분석ALK 변이 폐암세포(H3122) 4,835개와 항암제 내성 폐암세포(LR) 4,566개를 단일세포 RNA 시퀀싱 분석하여, CDA의 발현이 내성 세포에서 증가함을 확인.약물 투여 전 암세포에서도 CDA발현이 높은 세포가 소수지만 이미 존재함을 알 수 있다. |
□ 연구배경
○ALK 유전자 돌연변이 폐암의 치료제로 세리티닙과 같은 ALK 저해제가 탁월한 치료 효과를 보이지만, 1년 이내에 내성이 발생하고 암이 재발하는 심각한 문제점이 있음
○기존의 유전체분석은 수백만 개 세포를 한꺼번에 갈아서 분석함으로써 암세포의 이질성을 반영할 수 없는 한계가 있었음
○최근 단일세포 유전체 분석기술의 발달로 개별세포 하나하나의 유전자 발현 분석이 가능해짐으로써 항암제 내성의 원인이 되는 희귀 암세포를 구별해 내는 연구가 가능함
□ 연구내용
○이 연구에서 항암제 내성 폐암세포 모델의 단일세포 RNA 시퀀싱 분석을 통해, 피리미딘 회수경로 효소인 시티딘 탈아미노효소(CDA)의 발현이 높은 암세포가 항암제 내성이 생기는 과정에서 선택적으로 살아남는 것을 확인함
○CDA 발현이 높은 암세포는 빠르게 증식할 뿐만 아니라, 암 전이를 조절하는 전사인자의 활성으로 인해 암세포의 이동성과 침윤성이 높아짐
○내성 암세포에 CDA 발현을 감소시키자, 암세포의 증식이 감소하였으며, 세포 이동성과 침윤성이 감소하고, 항암제에 대한 민감성이 회복되는 것을 발견함
○CDA 억제제인 테트라하이드로우리딘 또는 CDA 유도 대사를 표적으로 하는 5-formyl-2'deoxycytidine(5fdC)는 CDA 발현이 높은 항암제 내성 암세포를 선택적으로 사멸시킬 수 있음을 발견함
□ 연구성과의 의미
○ 난체성 폐암의 항암제 내성 원인 규명 및 새로운 치료 표적 발굴- ALK 표적항암제에 대해 내성이 발생한 폐암 환자 중, CDA 발현이 높은 환자를 선별하여 CDA 억제제를 기존 항암제와 병용투여 함으로써 항암제 내성을 극복할 수 있는 새로운 치료법으로 개발될 가능성을 시사함
□용어해설
1. 항암제 내성(Cancer drug resistance)◦ 암 환자에게 항암제를 지속적으로 투여하면, 항암제에 대한 민감성이 떨어지고 암세포가 증식하게 되어 암이 재발되는 현상
2. 단일세포 유전체분석(Single cell genomics)◦ 기존의 유전체분석은 조직 내의 다양한 세포를 한꺼번에 갈아서 분석하기 때문에 개별 세포의 유전체분석이 불가능했음. 단일세포 유전체분석은 세포 하나하나의 유전체 프로파일링이 가능한 기술임
3. ALK 변이 폐암(ALK fusion positive lung cancer)◦ 폐암의 대부분을 차지하는 비소세포폐암 중 ALK 유전자의 돌연변이가 발생한 폐암임. ALK 변이 폐암은 비소세포폐암의 약 5%이며 비흡연자 그리고 젊은 연령대에서도 빈번히 나타나기 때문에 치료제 개발이 시급함. ALK 변이를 표적으로 하는 항암제는 현재 3세대까지 개발되어 임상에서 높은 효율을 보이고 있으나, 치료 1-2년 이내에 내성이 발생하는 문제점이 있음.
4. 시티딘 탈아미노효소(cytidine deaminase, CDA)◦ DNA와 RNA의 분해 중에 형성되는 핵 염기와 뉴클레오사이드를 복구하는 피리미딘 회수경로에서 CDA가 주요 효소로 작용함. 본 연구에서 항암제 내성 암세포에서 CDA의 발현이 높으며, CDA 발현이 높은 암세포는 핵산 분해과정에서 생성된 염기와 뉴클레오시드를 재활용하는 회수경로를 활성화시켜, 세포 분열이 활발하고 세포 이동성 및 침윤성이 높아짐을 발견함. CDA를 억제하는 약물을 내성 암세포에 처리하면 항암제에 대한 민감성이 회복됨을 발견함. 본 연구를 통해 CDA를 항암제 내성을 극복할 수 있는 새로운 치료 표적으로 제시함
한국생명공학연구원 홍보실 제공
노벨사이언스 science@nobelscience.co.kr
<저작권자 © 노벨사이언스, 무단 전재 및 재배포 금지>



 간단한 공정으로 이산화탄소 분리 성공
간단한 공정으로 이산화탄소 분리 성공








